ENT : Autres Sites
- Bulletin Officiel (B.O.)
- Comptes de Courrier Electronique Professionnel
- Conseil Supérieur des Programmes (C.S.P.)
- ENT Académique (e-Lyco)
- Espace de Stockage de Fichiers
- Gestion En Ligne des Activités Pédagogiques de l'Accompagnement Personnalisé (GEL2AP)
- Le calendrier scolaire
- Mon Pearltrees (Ma collection de favoris)
- Sujets zéro en classe de première pour le baccalauréat 2021
Étiquettes
addons ADN allèle ARNm bactérie biodiversité biomasse cancer caryotype cellule contraception hormonale devoir embryon génotype génétique interphase lithosphère matière vivante mitose molécule organique mucoviscidose mutation métabolisme métabolisme cellulaire nucleotide oeil oestradiol ovocyte photosynthèse phénotype plugins primates protéine réplication santé sol sélection naturelle séquence nucléotidique tectonique traduction transcription translation vision wordpress écosystèmeLexique - Glossaire - Dictionnaire - Encyclopédie
- Dictionnaire de l'Encyclopædia Universalis
 Dictionnaire Encyclopédique Environnement
Dictionnaire Encyclopédique Environnement Dictionnaire Environnement
Dictionnaire Environnement- Dictionnaire Larousse
- Encyclopedia of Earth (anglais)
- GEOL-ALP : GLOSSAIRE GÉOLOGIQUE
- Géologues Prospecteurs – Dictionnaire illustré de Géologie
- Glossaire bilingue de géologie
- Lexique – CNRS
- Lexique (niveau : Lycée) [site : Assistance scolaire personnalisée]
- Termsciences, portail terminologique
Archives pour l'étiquette mutation
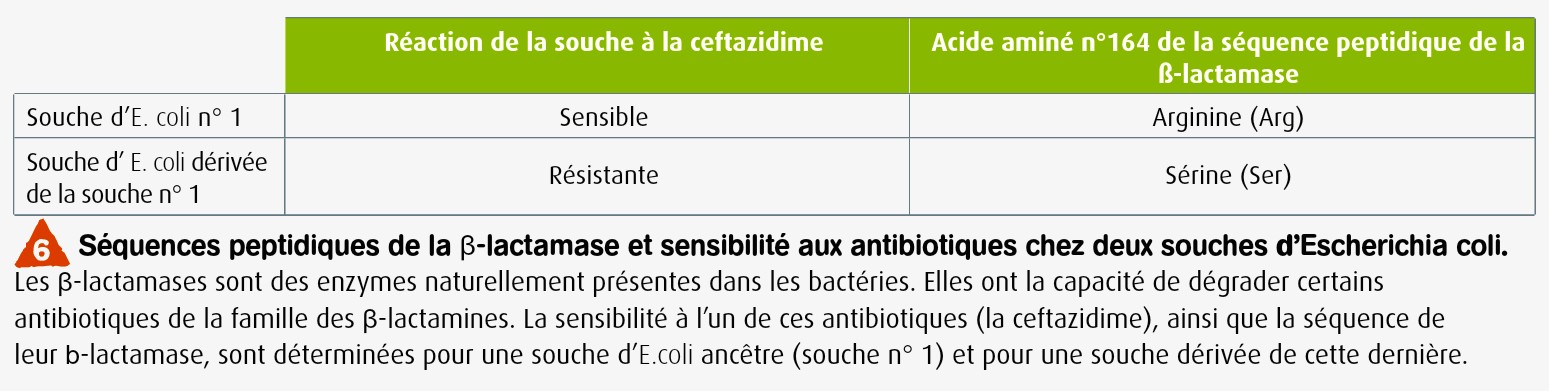
D2 – Origine d’une résistance bactérienne à un antibiotique
A partir d’informations tirées du document 6 page 273 du livre d’une part, et de vos connaissances d’autre part, démontrez que la résistance bactérienne à une substance antibiotique a pour origine une mutation.
D’après le document, nous constatons que la séquence polypeptidique de l’enzyme β-lactamase de la bactérie E. coli dérivée de la souche n°1 diffère de celle de la même enzyme de la souche E. coli initiale n°1 au niveau de l’acide aminé n°164. Il y a une substitution Arg 164 Ser.
Or nous savons que les propriétés biologiques d’une protéine – donc d’une enzyme – dépendent de cette séquence polypeptidique.
De plus nous savons que chacun des acides aminés de cette séquence est déterminé par un codon de nucléotides de l’ARNmessager, lors de la traduction de ce dernier.
Enfin nous savons que la séquence nucléotidique d’un ARNm dépend de celle de l’allèle d’un gène donné lorsque ce dernier est transcrit.
Ce qui fait que toute modification de la séquence nucléotidique du brin transcrit de l’ADN – c’est à dire toute mutation – aura donc une répercussion sur la séquence nucléotidique de l’ARNm et donc ensuite peut avoir une répercussion sur la séquence polypeptidique.
Si par exemple il s’est produit la mutation TCT xxxx TCA ou TCC xxxx TCG au niveau du brin transcrit de l’ADN bactérien, alors au niveau de l’ARNm nous aurons : AGA www AGU ou AGG www AGC, et donc nous aurons Arg 164 Ser au niveau de la séquence polypeptidique de l’enzyme β-lactamase.
Et comme la synthèse d’un enzyme β-lactamase avec Ser au lieu de Arg confère à la bactérie”mutée”une résistance à l’antibiotique “ceftazidime”, nous pouvons donc en conclure que, d’une façon générale, la résistance bactérienne a une substance antibiotique provient bien au départ d’une mutation au niveau d’un gène de l’ADN bactérien.
On cherche à déterminer si c’est le contact de la bactérie avec la substance antibiotique qui est à l’origine des mutations qui lui confère une résistance.
B.31 – Phénotype cancéreux
Travail préparatoire
https://goo.gl/forms/IJbwUYpJ3VQ6Q4Cj2
Travail d’investigation
Travail de bilan notionnel
Travail d’auto-évaluation
3B2. Perturbation du génome et cancérisation
-
De quelle façon des cellules somatiques saines deviennent-elles cancéreuses ?
-
Quelle est la composante génétique de la cancérisation ?
-
Quelle est la composante environnementale de la cancérisation ?
- Activité d’exploitation de documents
Documents 1, 2 et 3 page 264, et 6, 7 page 265.
Présenter les étapes qui conduisent à un phénotype cancéreux.
-
Notions à acquérir
-
Compétences à développer
…
C.2 – Impact des mutations sur la biodiversité
-
En quoi les mutations contribuent-elles à créer de la biodiversité ?
- Etude de la biodiversité au sein de l’espèce Sus scrofa – Document de travail – Ressources : pour SeaView – pour Anagène/Géniegen
- Au sein d’une même espèces les individus présentent des variations phénotypiques. La comparaison des génotypes montrent des variations au niveau de gènes. Ces variations ou allèles résultent de mutations.
- La diversité des groupes sanguins chez les êtres humains
C.1 – Nature, origine et fréquence des mutations
- Précédemment nous avons comparé le phénotype d’un individu atteint de mucoviscidose et à celui d’une personne non atteinte.
- Nous avons constaté qu’à l’échelle moléculaire, ce phénotype avait pour origine une protéine CFTR non fonctionnelle dans un cas et une protéine CFTR fonctionnelle dans l’autre.
- De plus nous avons vu que les cellules réalisent la synthèse d’une protéine à partir de l’information résidant dans la séquence nucléotidique d’un gène.
- Nous pouvons donc émettre l’hypothèse que la séquence nucléotidique du gène de la CFTR d’une personne atteinte de mucoviscidose est différente de celle du gène de la CFTR d’une personne non atteinte.
- Entrainement ECE : Proposer une démarche expérimentale permettant de vérifier cette hypothèse.
10 minutes maxi.
[Réponse sur Padlet] - Pour la suite, regarder la démarche proposée reçue par email. (adresse du domaine lyceesaintmartin.org).
- Entrainement ECE : Proposer une démarche expérimentale permettant de vérifier cette hypothèse.
-
A quoi sont dues ces modifications de la séquence nucléotidique d’un gène ?
-
Qu’est-ce qu’une mutation ponctuelle ?
-
Quelles sont les différents types de mutations ponctuelles ?
-
A quel moment de la “vie” d’une cellule surviennent-elles ?
-
A quelle fréquence ?
-
A quelles conditions des modifications d’une séquence nucléotidique sont-elle “conservées” et deviennent des mutations ?
-
A quelles conditions une mutation va-t’elle “influer” sur le phénotype ?
-
A quelle condition une mutation va-t’elle être transmise “héréditairement” ?
-
Activité C11 – Caractéristiques d’une mutation [Fiche Connaissances]
-
Activité C12 – Activité Pratique : Le phénotype Xeroderma pigmentosum (mise en évidence de l’existence d’un système de réparation de l’ADN).
-
Connaissances à maîtriser
- notions de mutation ponctuelle, insertion, délétion, substitution
- mutation : naturelle, rare, aléatoire
- erreurs d’appariement ou lésions de l’ADN non corrigées par le “système de réparation” de l’ADN
- Impact sur le phénotype si une mutation touche la séquence d’un gène (exon)
- Transmission héréditaire si la mutation touche une cellule germinale.
-
Compétences requises
- mettre en relation des connaissances et des informations issues d’une document ou d’une démarche expérimentale pour déterminer la nature de la mutation responsable d’un phénotype particulier.
-
Capacités attendues
- utiliser les fonctionnalités d’un logiciel de traitement de séquences pour déterminer les caractéristiques de séquences nucléotidiques et comparer ces séquences
Activité Pratique “Type ECE” – La mucoviscidose
Déterminer l'origine génétique d'un cas de mucoviscidose.
:: Mutations (insertion, délétion) et Expression du programme génétique :: [Anglais]
:: Mutation ponctuelle ::
- Mutation ponctuelle : modification de la séquence nucléotidique d’un gène qui impacte entre un et dix nucléotides.
- On distingue trois formes de mutations ponctuelles :
- mutation par insertion,
- mutation par délétion,
- mutation par substitution.
B – Mutation, biodiversité et santé
Statistiques |
||
[hana-code-insert name='Statistiques Dcs Cancer France' /] |
[hana-code-insert name='Statistiques Cancer peau' /] |
[hana-code-insert name='Statistiques antibiotiques france' /] |
Plan du cours - Activités
- B1 – Modification phénotypique chez Saccharomyces cerevisiae
- B2 – Mutation et résistance bactérienne aux antibiotiques
- B3 – Mutation et maladie génétique
- B4 – Mutation et cancérisation
B1 – Modification phénotypique chez Saccharomyces cerevisiae
- Diaporama présenté en cours
- Introduction (pratiquer un raisonnement scientifique)
- Travaux Pratiques “type ECE”
- Fiche sujet (1/2) [pdf]
- Fiche sujet (2/2) et fiche protocole [pdf]
- Fichiers de séquences nucléotidiques [zip]
- Logiciel “GenieGen” [téléchargement] – Fiche technique ” GenieGen”
B2 – Mutation et résistance bactérienne aux antibiotiques
- Qu’est-ce qu’un antibiotique ?
- Quel est son mode d’action ?
Les antibiotiques, la révolution médicale du 20ème siècleLes antibiotiques sont des molécules naturellement synthétisées par des microorganismes pour lutter contre des bactéries concurrentes de leur environnement. Il existe aujourd’hui plusieurs familles d’antibiotiques composées de molécules naturelles, semi-synthétiques ou de synthèse, qui s’attaquent spécifiquement à une bactérie ou un groupe de bactéries. Certains antibiotiques vont agir sur des bactéries comme Escherichia Coli dans les voies digestives et urinaires, d’autres sur les pneumocoques ou sur Haemophilus influenzae dans les voies respiratoires, d’autres encore sur les staphylocoques ou les streptocoques présents au niveau de la peau ou de la sphère ORL. Les antibiotiques, spécifiques des bactériesLes antibiotiques ne sont efficaces que sur les bactéries et n’ont aucun effet sur les champignons et les virus. Ils bloquent la croissance des bactéries en inhibant la synthèse de leur paroi, de leur matériel génétique (ADN ou ARN), de protéines qui leur sont essentielles, ou encore en bloquant certaines voies de leur métabolisme. Pour cela, ils se fixent sur des cibles spécifiques. Largement utilisés depuis la seconde guerre mondiale, les antibiotiques ont permis de faire considérablement reculer la mortalité associée aux maladies infectieuses comme la tuberculose ou la peste au cours du 20ème siècle. Source: http://www.inserm.fr |
- Comment mettre en évidence l’action d’un antibiotique ?
- Comment se manifeste la « résistance » bactérienne aux antibiotiques ?
- Antibiogramme : Technique de réalisation [vidéo]
- Travaux Pratiques – Modélisation antibiogramme :: Mise en évidence de la sensibilité ou résistance d’une souche bactérienne à un antibiotique ::
- Quelle est l’origine de cette « résistance » ?
- L’hypothèse d’une mutation
- Problème : la mutation précède-t-elle le contact de la bactérie avec l’antibiotique ? Ou l’antibiotique induit-il la mutation ? Raisonnement et expérience de Miloslav Demerec.
B3 – Mutation et maladie génétique
-
Le cas de la mucoviscidose [Diaporama]
-
- Exposé de connaissances – Définition d’un phénotype pathologique à l’échelle macroscopique, microscopique et moléculaire.
- Notion de Protéine
- Exercice – Montrez que dans le cas d’un phénotype pathologique comme la mucoviscidose, le phénotype macroscopique s’explique par le phénotype microscopique qui lui-même s’explique par le phénotype moléculaire (ou que le phénotype moléculaire explique le phénotype microscopique qui lui-même explique le phénotype macroscopique).
- Travaux Pratiques – Déterminer l’origine de la mucoviscidose, montrer l’existence d’une relation entre le génotype d’un patient et son phénotype.
- Activité Complémentaire – Traitement de données moléculaires [Rastop]
- Le cas du diabète de type II [Diaporama]
B4 – Mutation et cancérisation
- Qu’est-ce qu’une cellule cancéreuse ?
Une tumeur cancéreuse ?
Des métastases ?
Qu’est ce que la cancérisation ? - Étude des documents :
- 7 page 267,
- 1, 2 et 3 page 264,
- 4 et 7 page 265
- Quelles mutations sont plus fréquentes dans le cas d’un cancer ?
Quelles techniques permettent de mettre en évidence les gènes concernés ? - Étude des documents :
- 1, 2 et 3 page 266
- 4, 5 et 6 page 267.
- Le cas du cancer du poumon – Étude d’un article de presse
- Le cas du cancer du col de l’Utérus –
Documents complémentaires
-
Article à lire.
-
Animations.
-
Vidéos.
+
+
+
+
+
+
+
-
Fichiers de données
- Données moléculaires
- Mucoviscidose –
- Modèle théorique de la structure de la CFTR sauvage (=”normale”)
- Des représentations anciennes de la protéine : avant que toute la structure de la molécule ne soit modélisée, les premières tentatives de modélisation tridimensionnelle du domaine NB1 de la CFTR humaine ont été réalisées sur des peptides synthétiques, ne représentant qu’une portion du domaine. On sait aujourd’hui que les structures adoptées par les peptides ne reproduisent pas les conformations observées pour ces mêmes peptides au sein des domaines protéiques qui les contiennent, en raison de l’absence des contacts existant à grande distance sur la séquence.[source] – Protéine CFTR Normale (sauvage) – Protéine CFTR mutée (ΔF508)