SUJETS
1)- Restitution de connaissances
Indiquez de quoi est constituée la matière vivante (donnez au moins trois exemples de molécules) [3 points]
2)- Application de connaissances
QCM – Pour chaque item, cochez la réponse qui vous semble correcte parmi les quatre propositions. [2 points]
Version 1
|
Item A – Après une semaine passée dans une étuve à 40°c, un échantillon de salade verte qui pesait initialement 100g, ne pèse plus que 13g. On brûle ces 13g, et il ne reste que 0,8g de « cendres » constituées des éléments chimiques suivants : N, S, O, Na, Ca, Mg, Fe, Cl.
D’après les informations données ci-avant, le pourcentage de molécules organiques dans la salade est :
|
Item B – Parmi les molécules qui suivent quelle est celle qui n’est pas une molécule organique.
|
- ⬜ 13,8%
- ⬜ 12,2%
- ⬜ 86,2%
- ⬜ 87,8%
|
- ⬜ la thymine C5H6N2O2
- ⬜ l’olivine (Mg,Fe)2[SiO4]
- ⬜ l’héparine C12H19NO20S3
- ⬜ la leucine C6H13NO2
|
Version 2
|
Item A – Après une semaine passée dans une étuve à 40°c, un échantillon de salade verte qui pesait initialement 100g, ne pèse plus que 12g. On brûle ces 12g, et il ne reste que 0,5g de « cendres » constituées des éléments chimiques suivants : N, S, O, Na, Ca, Mg, Fe, Cl.
D’après les informations données ci-avant, le pourcentage de molécules organiques dans la salade est :
|
Item B – Parmi les molécules qui suivent quelle est celle qui est une molécule organique.
|
- ⬜ 11,5%
- ⬜ 12,5%
- ⬜ 88,5%
- ⬜ 87,5%
|
- ⬜ l’aragonite CaCO3
- ⬜ l’olivine (Mg,Fe)2[SiO4]
- ⬜ la kaolinite Al2Si2O5(OH)4
- ⬜ la thymine C5H6N2O2
|
3)- Pratiquer un raisonnement expérimental – Concevoir un protocole pour apporter une réponse à un questionnement.
|
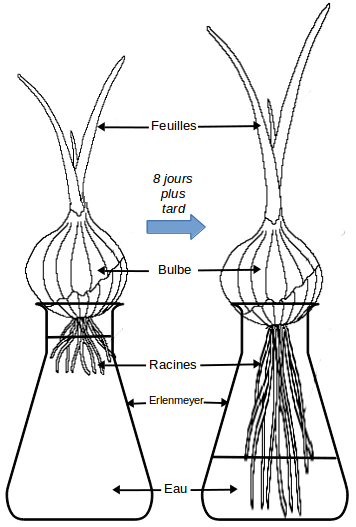
Examiner le croquis ci-contre. On a placé un bulbe d’oignon au niveau du col d’un erlenmeyer rempli d’eau. Les racines de l’oignon trempent dans l’eau. Huit jours plus tard on constate que le niveau de l’eau dans l’erlenmeyer a baissé.
On cherche à savoir ce qu’est devenue l’eau qui a « disparu » dans l’erlenmeyer, au bout de 8 jours.
On écarte l’hypothèse d’une « fuite par évaporation » dans la mesure où l’on a utilisé un mastic étanche entre les bords du col de l’erlenmeyer et le bulbe d’oignon.
M. GRUYONT émet l’hypothèse selon laquelle le bulbe d’oignon a absorbé l’eau par ses racines et a conservé ensuite la totalité de cette eau.
Mme BRAPEND émet l’hypothèse selon laquelle le bulbe d’oignon a absorbé l’eau par ses racines, puis l’eau est montée jusqu’aux feuilles et s’est totalement évaporée dans l’air en sortant des feuilles.
Pour l’une de ces deux hypothèses seulement, proposer un complément au protocole expérimental ci-contre permettant de savoir si cette hypothèse est correcte ou non.
Pour cela on dispose d’une balance de précision.
Attention ! Il ne s’agit pas de donner son avis sur l’hypothèse, de dire si elle est vraie ou non, à partir de « résultats inventés » !
|
 |
CORRIGÉ
1)- Indiquez de quoi est constituée la matière vivante (donnez au moins trois exemples de molécules) [3 points]
La matière vivante est constituée des mêmes éléments chimiques que la matière inerte mais dans des proportions différentes.
En particulier la matière vivante comporte davantage de carbone (C), d’hydrogène (H) et d’azote (N) que la matière inerte.
La matière vivante est un mélange hétérogène de molécules : elles est constituées de molécules organiques et de molécules minérales.
Les molécules organiques sont propres à la matière vivante. Il en existe quatre catégories : les glucides (ex : glucose), les protides, les lipides et les acides nucléiques (ADN).*
L’eau est la principale molécule minérale constitutive de la matière vivante (entre 60 et 70 % de la masse).
Vocabulaire scientifique
- matière
- molécule
- éléments chimiques
Erreurs scientifiques rencontrées dans les copies :
- confusion entre “éléments chimiques” et “molécules”
- confusion entre “molécule” et “matière”
2)- QCM – Pour chaque item, cochez la réponse qui vous semble correcte parmi les quatre propositions. [2 points]
Item A
Masse totale de la salade verte = masse des molécules organiques + masse des molécules minérales.
D’où :
masse des molécules organiques = Masse totale de la salade verte – masse des molécules minérales.
D’après le protocole suivi :
- le passage à l’étuve, retire l’eau de la salade. Donc masse d’eau = masse de la salade fraîche (100g) – masse de la salade “sèche” (13 ou 12 g). Or l’eau est une molécule minérale.
- la combustion de la salade “sèche” donne des “cendres” constitués d’éléments chimiques qui ne sont pas ceux des molécules organiques (C, H). Les “cendres” sont donc des molécules minérales. Leur masse (0,8 ou 0,5 g) s’ajoute à celle de l’eau.
Donc :
masse des molécules organiques = 100 g – (.87 + 0,8) g = 12,2 g
ou
masse des molécules organiques = 100 g – (.88 + 0,5) g = 11,5 g
Item B – Parmi les molécules qui suivent quelle est celle qui n’est pas une molécule organique. Réponse attendue : l’olivine (Mg,Fe)2[SiO4]
ou
Item B – Parmi les molécules qui suivent quelle est celle qui est une molécule organique. Réponse attendue : la thymine C5H6N2O2
3)- Pratiquer un raisonnement expérimental. Concevoir un protocole pour apporter une réponse à un questionnement. [5 points]
Critères d’évaluation
Le protocole proposé comporte :
- une 1ere étape :
- de mesure d’une masse initiale.
La valeur de la mesure en g sera (notée et) affectée à une variable (ex Mi) ;
- de mise en place du dispositif.
- une 2eme étape : un temps d’attente de 8 jours.
- une 3eme étape de mesure d’une masse finale. La valeur de la mesure en g sera (notée et) affectée à une variable (ex Mf).
- une 4eme étape d’exploitation des résultats : mise en relation (comparaison) de Mi et Mf en vue d’éprouver l’hypothèse choisie (Si Mi = Mf, alors l’hypothèse est ….)
Exemple. Pour mettre à l’épreuve l’hypothèse de M. GRUYONT (le bulbe d’oignon a absorbé l’eau par ses racines et a conservé ensuite la totalité de cette eau).
- 1ere étape :
- Mise en place du dispositif : remplir l’erlenmeyer d’eau, placer le bulbe d’oignon au niveau du col de l’erlenmeyer en veillant à ce que les racines trempent dans l’eau. Mettre un mastic étanche entre le bulbe et le col du récipient pour empêcher les fuites par évaporation.
- Mesure de la masse initiale du dispositif complet (erlenmeyer, bulbe d’oignon, eau, mastic) avec la balance de précision. La valeur de la mesure en g sera affectée à la variable Mi .
- une 2eme étape : Attente de 8 jours.
- une 3eme étape : mesure de la masse finale du dispositif. La valeur de la mesure en g sera affectée à la variable Mf .
- une 4eme étapae : exploitation des résultats. Si Mi = Mf, (conservation de la masse du système) alors l’hypothèse est M. GRUYONT est validée. Le bulbe d’oignon a absorbé l’eau par ses racines et a conservé ensuite la totalité de cette eau. Il n’y a ni perte, ni gain de masse.
Exemple. Pour mettre à l’épreuve l’hypothèse de Mme BRAPEND (le bulbe d’oignon a absorbé l’eau par ses racines, puis l’eau est montée jusqu’aux feuilles et s’est totalement évaporée dans l’air en sortant des feuilles).
- 1ere étape :
- Mesure de la masse initiale du bulbe d’oignon avec la balance de précision. La valeur de la mesure en g sera affectée à la variable Mi .
- Mise en place du dispositif : remplir l’erlenmeyer d’eau, placer le bulbe d’oignon au niveau du col de l’erlenmeyer en veillant à ce que les racines trempent dans l’eau. Mettre un mastic étanche entre le bulbe et le col du récipient pour empêcher les fuites par évaporation.
- une 2eme étape : Attente de 8 jours.
- une 3eme étape : mesure de la masse finale du bulbe d’oignon. La valeur de la mesure en g sera affectée à la variable Mf .
- une 4eme étape : exploitation des résultats. Si Mi = Mf, (conservation de la masse du bulbe d’oignon) alors l’hypothèse est Mme BRAPEND est validée. Le bulbe d’oignon a absorbé l’eau par ses racines puis l’eau est montée jusqu’aux feuilles et s’est totalement évaporée dans l’air en sortant des feuilles. Il n’y a ni perte, ni gain de masse.


 Dictionnaire Encyclopédique Environnement
Dictionnaire Encyclopédique Environnement Dictionnaire Environnement
Dictionnaire Environnement